ポイント
- α-アミノ酸の一種で,効率的な合成法が存在しないα,α-ジフルオログリシンの化学合成に成功。
- α,α-ジフルオログリシンの合成経路をコンピュータが予測し,合成化学実験により実証。
- 計算科学主導の合理的な新反応開発が実現。その更なる発展に期待。
概要
北海道大学創成研究機構化学反応創成研究拠点(WPI-ICReDD)の美多 剛特任准教授及び同拠点拠点長・同大学院理学研究院化学部門の前田 理教授らの研究グループは,コンピュータ上で可能性のある反応経路を予測し,得られた計算結果を合成化学実験によって具現化することで,α-アミノ酸*1の一種であるα,α-ジフルオログリシン*2の化学合成に成功しました。
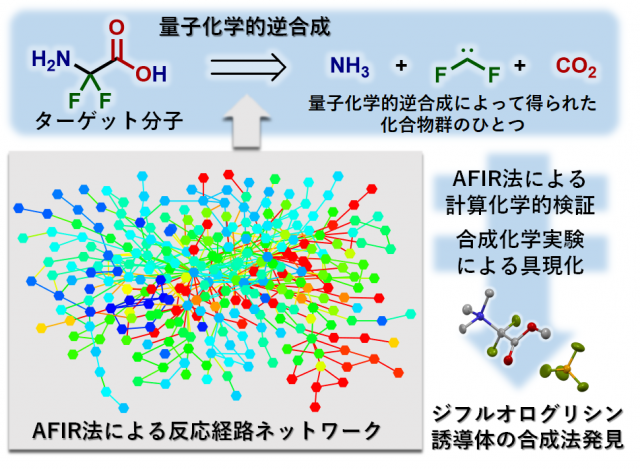
従来の有機合成化学に立脚した新反応開発では,有機合成化学者の経験や合成的なセンスが必要であることに加え,年単位に及ぶ膨大な実験が必要とされてきました。そのため,一つの革新的な反応の開発にかかる時間や費用が研究者にとって大きな負担でした。それに対し,本学の新しい研究拠点であるICReDDの核心技術であるAFIR法(人工力誘起反応法)*3は,量子化学的逆合成解析*4と呼ばれる手続きによってターゲット分子の合成経路を網羅的に予測することができます。そのため,ターゲット分子の合成が可能かどうか,可能な合成経路の化学収率はどの程度か,といったことを,予めコンピュータ上で予測することができます。したがって,長時間を要する実験的な反応条件の検討を省略することが可能であり,開発時間の大幅な短縮が見込まれることから,本手法を活用してグリシンの生物学的等価体*5であるα,α-ジフルオログリシン(これまでに効率の良い化学合成法が存在しない)の化学合成に取り組みました。その結果,わずか2か月という短期間で,その化学合成を達成しました。本手法はこれまでに先例のない合成戦略であり,次世代型の「計算による合成経路予測−合成実験による実現」の端緒を開くものであります。
なお,本研究成果は,日本時間2020年5月22日(金)公開のChemical Science誌のオンライン版にEdge Articleとして掲載されました。
また,本研究は,文部科学省科学研究費補助金「基盤研究C」(18K05096),「JST, CREST (新機能創出を目指した分子技術の構築)」(JPMJCR14L5),「JST, さきがけ(理論・実験・計算科学とデータ科学が連携・融合した先進的マテリアルズインフォマティクスのための基盤技術の構築)」(JPMJPR16N8),「JST, ERATO(前田化学反応創成知能プロジェクト)」(JPMJER1903),「文部科学省世界トップレベル研究拠点プログラム(WPI)」,「アステラス病態代謝研究会」の支援のもとで行われました。
計算科学主導によるジフルオログリシン誘導体の化学合成
【背景】
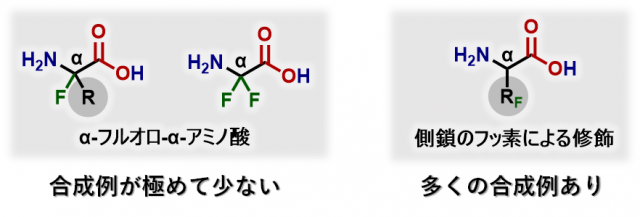
α-アミノ酸は生命を形作るペプチドやタンパク質の構成単位であるとともに,栄養補助剤,食品添加物などにも含まれており,我々の生活に必要不可欠な有機化合物です。有機合成化学においても,生物活性物質や医農薬品の合成中間体として頻繁に利用されています。自然界に存在する天然型α-アミノ酸は主に安価な発酵法*6により合成されていますが,その他の非天然型α-アミノ酸は,主に化学合成によって提供されています。しかし,非天然型α-アミノ酸が導入されたペプチドは,天然のペプチドには見られない新たな生物活性が期待されるため,入手容易な原料を用いた効率の良いα-アミノ酸の合成研究は現在でも活発に行われています。そこで同研究グループは,非天然型α-アミノ酸のひとつであるα-フルオロ-α-アミノ酸の化学合成を目指して研究を開始しました。フッ素原子を有機化合物の骨格に導入することで代謝安定性の向上,体内動態の改善,生物活性の増強などの効果が見込まれることから,フルオロアミノ酸を生物活性ペプチド鎖やタンパク質に組み込むことにより,効果の増強及び改善が期待できます。これまでに,α-アミノ酸側鎖*7の炭素鎖へのフッ素原子の導入が数多く報告されてきましたが(図1右図参照),主鎖のα位にフッ素原子が導入されたα-フルオロ-α-アミノ酸の合成の成功例は非常に限定されていました(図1左図参照)。その中でも特に,α位に2つのフッ素原子を有するα,α-ジフルオログリシン(NH2-CF2-CO2H)には効率的な合成法が知られていなかったため,このα,α-ジフルオログリシンをターゲット分子として合成研究を開始しました。
【研究手法】
本研究では,従来の実験科学主導型ではなく,計算科学主導型の開発手順を採用しました(図2)。まず,AFIR法によってα,α-ジフルオログリシンの分解経路を網羅探索し,それら分解経路の逆反応としてα,α-ジフルオログリシンを与える合成経路を予測しました(反応経路ネットワーク図の作成)。この分解経路の網羅探索による合成経路の予測手続きを,量子化学的逆合成解析と呼びます。美多特任准教授らは,予測された合成経路の中から,出発物質の安定性,各反応の反応障壁,及び出発原料の入手容易性を考慮して有望なものを選択し,その経路に基づいて合成化学実験を開始しました。試薬を加える手順や当量,用いる溶媒とその量,固体原料の溶解度,低沸点化合物(ガス状物質)の取り扱い,反応の後処理の方法及び単離*8・精製方法はコンピュータで予測するのは困難なため,これらは有機合成化学者が随時実験による検討を加えました。その結果,合成化学実験を始めてわずか2か月でα,α-ジフルオログリシンの化学合成を達成しました。
【研究成果】
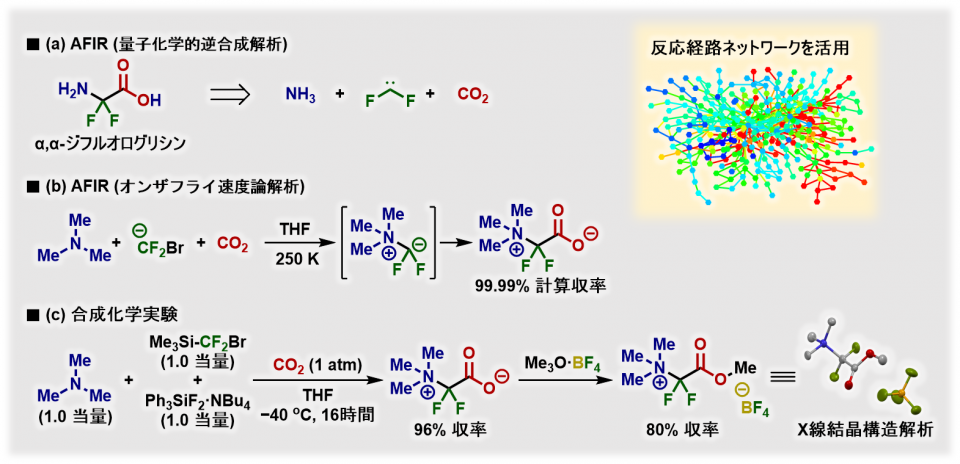
まず,AFIR法に基づく量子化学的逆合成解析によって,α,α-ジフルオログリシンの合成ルートを網羅的に探索しました。その結果,「アミン(NR3)」「ジフルオロカルベン(:CF2)*9」,及び「二酸化炭素(CO2)」といった単純かつ入手性の良い化合物群が見出され,これら3つの化合物は出発原料として適切でした(図3a)。この中でも特に二酸化炭素は地球温暖化物質として排出規制がなされている化合物です。そのため,二酸化炭素を有機化合物に導入するいわゆる二酸化炭素固定化反応の開発は,有機合成化学分野では重要な研究テーマのひとつです。一方で,ジフルオロカルベンは反応性が高く不安定な化学種のため,反応系内でジフルオロカルベンになる前段階の化合物(前駆体)から発生させる必要があります。そこで,実際に合成化学実験で使用するジフルオロカルベン前駆体(−CF2Br)とアミン化合物(R = Me)を用いて,AFIR法に基づくオンザフライ速度論解析*10によりα,α-ジフルオログリシン誘導体の化学収率を予測したところ,99.99%の化学収率で目的物が得られることがわかりました(図3b)。この計算結果を受けて,実験的に発生させた−CF2Br,NMe3,及びCO2の3成分を反応させたところ,これら3成分が連結したα,α-ジフルオログリシン誘導体(NMe3+-CF2-CO2−)が,予測値とほぼ同様の96%の化学収率で得られることがわかりました(図3c)。カルボン酸の状態では安定に取り出すことができなかったため,カルボン酸をメチルエステル化して結晶化させた結果,80%の化学収率でメチルエステル化体を単離することができました。一般にジフルオロカルベンは求電子的な性質を有するため,求核剤*11とは非常に良く反応します。そのため反応性の低く安定な求電子剤*12である二酸化炭素と効率良く反応することを予め予想することは困難であり,量子化学計算による予測があったからこそ見出された反応です。また,精度の高い量子化学計算により「目的物が99.99%の収率で得られた」という保証は重要な開発指針となり,初期検討で目的物が全く得られなかった際,実験を断念せず継続し,その原因は単離・精製方法にあることを明らかにする契機となりました。このように,計算科学による反応予測は,実験科学者に数多くの有益な情報を提供してくれたことから,より合理的な反応開発が可能となりました。
【今後への期待】
試行錯誤を実験の場のみに求めるのではなく,その多くを量子化学計算によって代替し,意味のある新反応を創出した本研究は,次世代型の有機合成研究と位置付けることができます。加えて,AFIR法を上手に活用することで,人知が及びにくい新しい合成経路を見出せることが実証されたため,今後の創薬資源・機能性物質などの効率的創出への展開が期待されます。現在,AFIR法で見出された合成経路のデータベース化を進めており,収録データ数は日々増加し続けております。そのデータベースを情報科学者と共有し活用することで,新反応開発がさらに加速されると共に,より複雑な反応系(触媒反応等)への適用が期待されます。
論文情報
論文名 Discovery of a Synthesis Method for a Difluoroglycine Derivative Based on a
Path Generated by Quantum Chemical Calculations(量子化学計算により見出され
た反応経路を基盤としたジフルオログリシン誘導体の化学合成)
著者名 美多 剛1,2,原渕 祐1,2,3,4,前田 理1,2,3,5(1北海道大学化学反応創成研究拠点
WPI-ICReDD),2 科学技術振興機構(JST) ERATO前田化学反応創成知能プロジェク
ト,3北海道大学大学院理学研究院化学部門, 4JST さきがけ, 5物質・材料研究機構 合型材
料開発・情報基盤部門(MaDIS))
雑誌名 Chemical Science(化学全般の専門誌)
DOI 10.1039/D0SC02089C
公表日 日本時間2020年5月22日(金)(オンライン公開)
お問い合わせ先
北海道大学創成研究機構化学反応創成研究拠点(WPI-ICReDD)
特任准教授 美多 剛(みたつよし)
TEL 011-706-9653 FAX 011-706-9655 メール tmita[at]icredd.hokudai.ac.jp
URL https://www.icredd.hokudai.ac.jp/ja/mita-tsuyoshi
北海道大学創成研究機構化学反応創成研究拠点(WPI-ICReDD)拠点長・同大学院理学研究院
化学部門 教授 前田 理(まえださとし)
TEL 011-706-8118 FAX 011-706-8118 メール smaeda[at]eis.hokudai.ac.jp
URL https://wwwchem.sci.hokudai.ac.jp/~theochem/
北海道大学総務企画部広報課(〒060-0808 札幌市北区北8条西5丁目)
TEL 011-706-2610 FAX 011-706-2092 メール kouhou@jimu.hokudai.ac.jp
【参考図】
図1. α-フルオロ-α-アミノ酸の種類
図2. 計算科学主導による反応開発
図3. ジフルオログリシン誘導体合成法の開発手順 (Meはメチル基(CH3)の略)
【用語解説】
*1 α-アミノ酸 … アミノ基とカルボキシ基の両方の官能基を持つ有機化合物の総称であり,カルボキシ基に隣接した炭素原子にアミノ基が結合したものを特にα-アミノ酸と呼ぶ。ペプチドやタンパク質の構成単位である。
*2 α,α-ジフルオログリシン … α-アミノ酸のうち最も単純な骨格であるグリシン(NH2-CH2-CO2H)のアミノ基とカルボキシ基で挟まれた炭素原子にフッ素原子が2つ結合している化合物(NH2-CF2-CO2H)。グリシンの生物学的等価体とされる。
*3 AFIR法(人工力誘起反応法) … 前田教授らが開発した量子化学計算に基づく反応経路探索法。反応する分子同士の間に人工的な力(人工力関数)を加え,反応経路を網羅的に探索する手法。
*4 量子化学的逆合成解析 … ターゲット分子(この場合はα,α-ジフルオログリシン)の異性化・分解経路を網羅探索し,それらの逆反応としてターゲット分子に至る出発物質と反応経路を予測する手続き。本研究では,異性化・分解経路の網羅探索にはAFIR法を用いた。
*5生物学的等価体 … 医薬分子において生物学的に同じ役割を果たす他の部分構造。生物活性化合物の主要活性に影響を与えることなく,化合物に含まれる官能基を他のものに置換することで,医薬特性が改善される。水素原子をフッ素原子に置換する戦略が多い。
*6 発酵法 … 微生物を培養する培地にグルコースなどの原料を入れ,微生物の増殖とともにα-アミノ酸を生産させる手法。非常に安価にα-アミノ酸を合成することができる。
*7 α-アミノ酸側鎖 … 構造式 (NH2-CHR-CO2H)で表されるRの部分。
*8 単離 … 様々なものが混合している状態にあるものから,その中の特定の要素のみを取り出すこと。
*9 ジフルオロカルベン(:CF2)… 価電子が6個でフッ素原子が2つ結合した中性な炭素
*10 オンザフライ速度論解析 … 反応経路探索と速度論解析を同時並行で実行し,出発物質から速度論的に進行可能な異性化・分解経路のみを網羅探索することで,どのような化合物がどれくらいの割合で生成するかを調べる手続き。本研究では,異性化・分解経路の網羅探索にはAFIR法を用いた。
*11 求核剤 … 電子を与える化学種。
*12 求電子剤 … 電子を受け取る化学種。代表的なものにカルボニル基がある。