ポイント
・電界非接触撹拌技術を用いて,がん細胞が動く時に重要なRac/Cdc42の活性化を検出。
・大腸がん患者から摘出した手術検体(がん組織)で,がん細胞の浸潤能・転移能の評価に成功。
・がん細胞のリンパ節転移の予測に期待。
概要
北海道大学大学院医学研究院腫瘍病理学教室/WPI-ICReDDの田中伸哉教授らの研究グループは,大腸癌患者から摘出された癌組織を用いて,患者それぞれの癌細胞が,どのくらい動く力を持っているのかを組織切片上で評価することに,世界で初めて成功しました。癌細胞が動く力(運動能・浸潤能)は,低分子量Gタンパク質のRacやCdc42*1によって制御されており,これらの分子が活性化されているほど癌細胞はよく動き,血管やリンパ管の中に侵入して転移しやすくなります。本研究では,外科手術によって摘出された大腸癌組織切片上(FFPE検体*2)で,活性化Rac/Cdc42に特異的に結合するプローブ溶液を,近年開発された電界非接触撹拌技術*3を用いて極めて高速に攪拌させることにより,迅速且つ特異的にRac/Cdc42活性を検出することに成功しました。
本研究により,細胞のRac/Cdc42活性は,①大腸の正常粘膜よりも腫瘍領域で有意に高いこと,②癌細胞のステージが上がるほど,Rac/Cdc42の活性が上昇すること,③特に癌細胞が周りの正常組織に浸潤していく先端部(invasive front)で高いことがわかりました。さらに,④Rac1/Cdc42活性が高い症例は,リンパ管浸潤をしやすい傾向があることがわかりました。この技術は,大腸癌のみならず,乳癌や脳腫瘍でも有用であり,がん患者の術後のフォローアップ,更にはRac阻害剤のコンパニオン診断において重要な情報を提供できると期待されます。
本技術は,迅速免疫染色研究会(R-IHC研究会)によって開発された技術を基盤としてさらに開発されたものであり,令和2年6月4日に特許(特許第6712810号)を取得しました。なお,本研究成果は,日本時間2022年2月2日(水曜)公開のScientific Reports誌に掲載されました。
以上の文章は北海道大学のプレスリリースの一部のみとなり、詳細は下記のプレスリリースと論文のリンクでご参照ください。
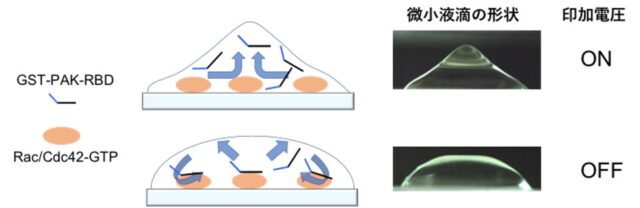
電界非接触撹拌技術による微小液滴の形状変化。低周波の電圧を繰り返し与え,GST-PAK-RBDプローブが入った液を高速でかき混ぜることで,癌細胞内の活性化Rac/Cdc42(Rac/Cdc42-GTP)にGST-PAK-RBDプローブを迅速且つ特異的に結合させることに成功した。

